Principe de la photographie interférentielle
AgBr
Les cristaux d’AgBr constituent le support des images enregistrées dans l’émulsion. Ce sont eux qui sont sensibles à la lumière.
La structure cristalline d’AgBr est de type cubique à faces centrées (comme NaCl) :
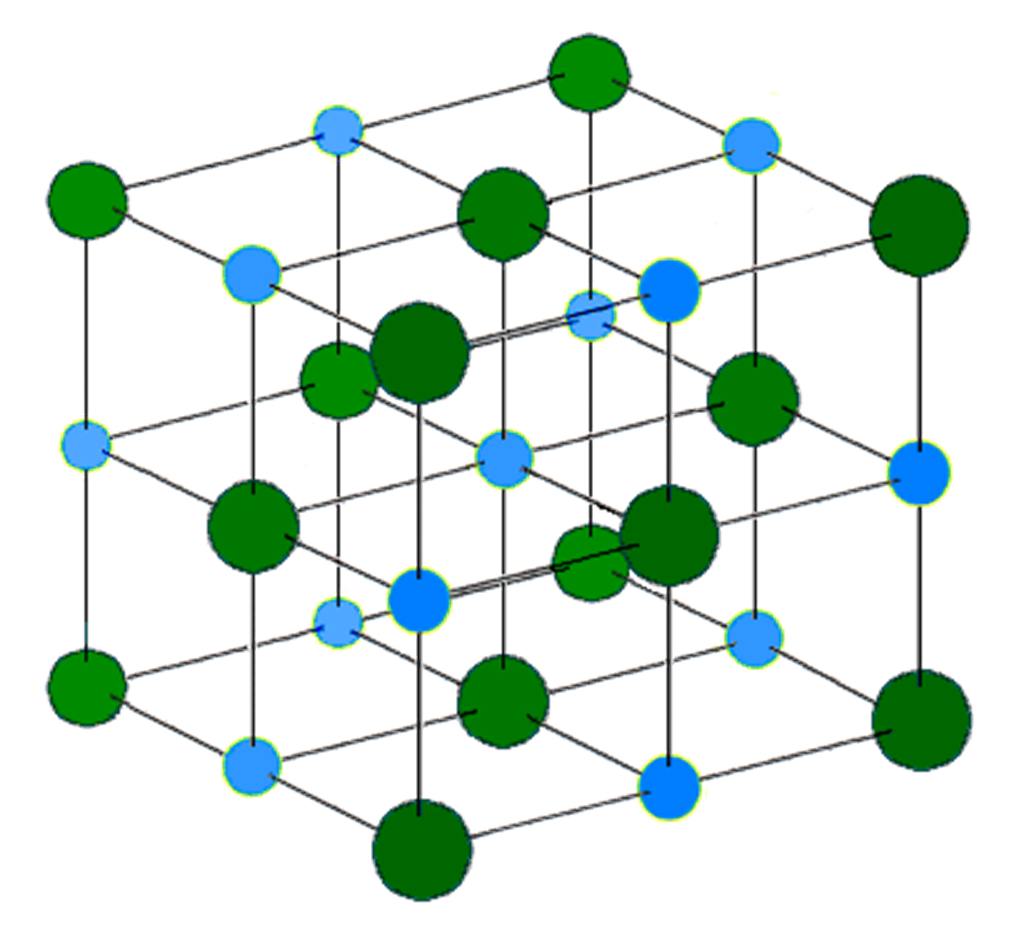
Les numéros atomiques sont 47Ag et 35Br.
Paramètre de maille : a ≈ 0.5774 nm à 25°C. Il y a 4 atomes d'argent par maille.
Dans la U04, les grains sont des nanocristaux d’AgBr assimilables à des sphères de 4 nm de diamètre. Il y a donc environ 7 mailles dans un diamètre de grain, soit 180 mailles dans un grain, et donc environ 700 atomes d’Ag.
La densité des grains d’AgBr dans une émulsion photographique est très élevée : on est typiquement dans un régime de nanoparticules quasi jointives. L’ordre de grandeur est donc de 1017 grains/cm3, soit 105/µm3. Dans une « colonne » de 4 µm de haut (l’épaisseur de l’émulsion) sur 1 µm de côté, on a donc 400 000 grains. À la limite de résolution de l’œil (100 µm), on a 4 milliards de grains.
Pour évaluer le nombre de nanocristaux dans un « miroir » de l’émulsion, il faut considérer le pas du réseau (λ/2n) à 400 nm, soit 130 nm. Dans une colonne de 1µm, on a donc, pour un réseau carré, 6500 grains dans une tranche de 65 nm d’épaisseur, et même encore 1000 dans une tranche de 10 nm.
La gélatine
La gélatine utilisée en photographie argentique est de la gélatine de collagène. L’indice optique est de l’ordre de 1.4 à 1.5.
Par rapport à la photographie couleur traditionnelle (PCT), la photographie Lippmann est plus exigeante sur la qualité de la gélatine :
| Propriété | PCT | Lippmann |
|---|---|---|
| Transparence | Importante | Critique |
| Homogénéité | Micron | Sub-micron |
| Gonflement | Acceptable | À minimiser |
| Diffusion interne | Peu critique | Catastrophique |
| Rôle optique | Passif | Actif |
La gélatine contient de l'eau. La gélatine sèche, avant la développement ou après séchage, contient une quantité d'eau qui dépend de l'humidité relative ambiante:
| Humidité relative ambiante | Teneur en eau |
|---|---|
| 20 % | 3-5 % |
| 40 % | 6-9 % |
| 60 % | 10-14 % |
| 80 % | 15-20 % |
L'effet de l'humidité ambiante sur la couleur interférentielle est un décalage de quelques nm.
Plongée dans l'eau, la gélatine l'absorbe massivement. L'eau peut occuper 50 à 75% du volume. En masse, 1 g de gélatine peut absorber de 1 à 3 g d'eau.
Le temps de diffusion de l'eau dans la gélatine peut s'écrire \[t = \frac{L^2}{D}\] où \( D_{\mathrm{eau}} \sim 10^{-6}\,\mathrm{cm^2/s} \). Pour 4 µm, on obtient 0.16 s. L'équilibre n'est atteint qu'après une relaxation mécanique, qui peut durer quelques dizaines de secondes, jusqu'à une minute.
L'arrivée massive d'eau peut casser des chaines polymères et entrainer une réorganisation mécanique du réseau polymère. La gélatine peut ainsi légèrement se contracter.
L'émulsion
L’émulsion est constituée de gélatine et de grains d’AgBr. En photographie couleur traditionnelle (PCT), on trouve aussi des colorants pour rectifier la sensibilité des émulsions aux différentes longueurs d’onde.
L'AgBr est sous forme solide dans la gélatine, il se dissout très peu dans l'eau (\( K_{sp}(AgBr)≈5×10^{−13} \)). Pour mémoire, \( K_{sp} \) décrit l'équilibre de \( \ce{AgBr <=> Ag+ + Br-} \).
L’épaisseur de l’émulsion est des l’ordre de 100µm en PCT, et 4 µm pour l’U04.
Réaction de l’AgBr avec la lumière
On peut modéliser l’AgBr comme un semi-conducteur, avec un gap de 2.5 eV (496 nm → cyan) à 2.7 eV (460 nm) entre la bande de valence et la bande de conduction.
Après l’excitation d’un électron, trou et électron se recombinent très vite (10-12 à 10-9 secondes). Mais des défauts présents dans le cristal peuvent piéger l’électron, qui peut alors se combiner à un \( \ce{Ag+}\) pour former un \( \ce{Ag^0}\).
Après exposition, plusieurs \( \ce{Ag^0}\) ont pu être créés dans un grain. Ils forment un amas microscopique d’argent, de quelques atomes, invisibles à l’œil nu : ce sont les centres latents, qui forment une image latente.
Noter que les Ag+ aqueux ne participent pas à l'image: ils sont trop peu nombreux.
Sensibilité de l’AgBr
Pour réaliser une photographie couleur, il faut que le cristal réagisse à toutes les longueurs d’onde du visible. En PCT, on ajoute des colorants sensibles aux longueurs d’onde plus élevées, qui produisent des électrons qui peuvent ensuite se combiner aux atomes d’Ag. En photographie Lippmann, ce n’est pas nécessaire : comme les grains deviennent très petits, les états de surface ne sont plus négligeables. Leur énergie, dans le gap, permet d’exciter les électrons avec de la lumière de plus grande longueur d’onde. Le courbe ci-dessous montre la sensibilité en longueur d’onde pour des émulsions traditionnelles (en bleu) et l’U04 (en orange).
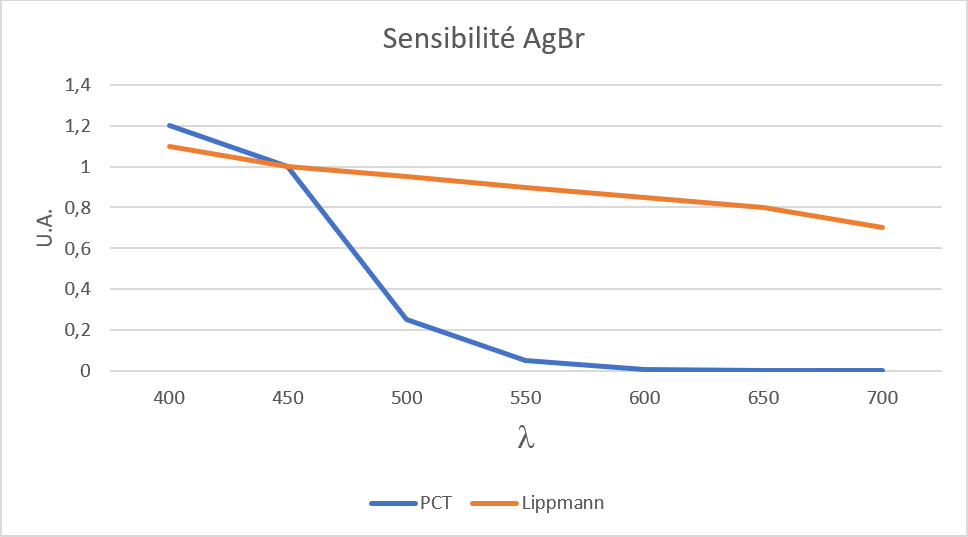
Yves Gentet donne une sensibilité S=0.6 mJ/cm² pour l’U04. Pour une intensité I exprimée en W/cm², on a directement le temps de pose T=S/I. Par exemple, pour I=1 mW/cm², T=0.6 s.
Enregistrement et révélation de l’image dans l’émulsion d’AgBr
Révélateur chimique
Le révélateur chimique traditionnel transforme tout le grain d’AgBr en \( \ce{Ag^0}\). Le premier révélateur à agir est la phénidone (notée ici \( \ce{PhH2}\)), qui s'oxyde en milieu alcalin: \[\ce{PhH2 -> Ph + 2H+ + 2e-}\]Les électrons libérés peuvent réduire des \( \ce{Ag+}\) en \( \ce{Ag^0}\). La réaction est autocatalytique: au voisinage d'un amas d'\( \ce{Ag^0}\) (centre latent), le potentiel redox est abaissé, la phénidone transfère un électron. L’\( \ce{Ag^0}\) existant sert de noyau de croissance, et le cristal se transforme petit à petit en agrégat métallique.
La réaction est donc autocatalytique, et d'autant plus rapide que l'agrégat est gros. S'il compte moins de 4 \( \ce{Ag^0}\), la réaction ne se produit pas; avec 5 à 8 atomes, elle se produit lentement, en 10-100ms; avec plus de 10 atomes, la réaction est rapide (1 ms et moins). À la fin du développement, tous les cristaux (grains) qui avaient un centre latent de plus de 3 ou 4 atomes sont devenus de l’argent métallique, les autres sont restés à l’état d’AgBr. Ces cristaux d’AgBr sont ensuite éliminés par le fixateur, qui les transforme en \( \ce{Ag+}\) et \( \ce{Br-}\) aqueux, c'est à dire dissous dans l'eau.
Le deuxième révélateur est l'hydroquinone (noté ici \( \ce{HQ}\)). Elle s'oxyde pour des pH plus élevés que la phénidone et a une énergie d'activation plus élevée. Elle va donc renforcer le développement des centres latents plus gros, et donc augmenter le contraste. Mais \( \ce{HQ}\) est aussi capable de réduire la phénidone oxydée, et donc de la régénérée. Alors que \( \ce{PhH2}\) seule est un révélateur rapide mais qui s'épuise vide, et que \( \ce{HQ}\) seule est un révélateur lent mais contrasté, \( \ce{PhH2 + HQ}\) est un révélateur stable, puissant et contrôlable.
Révélateur physique
En Lippmann, on ajoute un révélateur physique (le thiocyanate d’ammonium) qui dissout les cristaux d’AgBr pendant le développement:
\( \ce{AgBr (s) + SCN- (aq) <=> [Ag(SCN)] (aq) + Br- (aq)} \)
Le thiocyanate va donc dissoudre légèrement la surface des cristaux. Le temps caractéristique de cette réaction est de l'ordre de 10 à 100 ms. L'argent complexé diffuse dans la solution, et re-précipite préférentiellement sur l'\( \ce{Ag^0}\), c'est à dire sur un centre latent. Ces \( \ce{Ag+}\) à nouveau solides peuvent être réduits en \( \ce{Ag^0}\) par la phénidone. Le thiocyanate renforce donc les zones exposées.
En dissolvant les \( \ce{Ag+}\) au voisinage des centres latents, le thiocyanate entre en compétition avec la phénidone pour les centres latents au voisinage du seuil de l'autocatalyse: la réduction des \( \ce{Ag+}\) en \( \ce{Ag^0}\), lente, n’a pas le temps de se faire avant que les \( \ce{Ag+}\) ait été dissous par le thiocyanate. Par contre, les zones fortement exposées sont développées avant que le thiocyanate ait le temps de réduire \( \ce{Ag+}\), et dans ce cas, son rôle est au contraire d'augmenter la taille de l'agrégat d'\( \ce{Ag^0}\).
À la fin du traitement, les \( \ce{Ag^0}\) qui ne sont pas suffisamment nombreux pour former un amas stable, se dispersent, et peuvent même se ré-oxyder.
Au final, le thiocyanate a augmenté le contraste des franges, les transformant d’une sinusoïde en un quasi-créneau. Le résultat final dépend de l’exposition et de la compétition entre les deux révélateurs.
On peut ci-dessous jouer sur l'exposition pour voir ce que ça donne :
Exposition : 12.0
À noter également que les courbes ci-dessus correspondent à une photographie Lippmann prise avec un miroir (presque) totalement réfléchissant. Dans le cas d’une réflexion vitreuse, la situation peut être fort différente. En effet, la modulation d’intensité n’est plus que de +/- 20% autour de la valeur moyenne. Utiliser le bouton bascule ci-dessous pour voir le résultat ci-dessus.
La zone pour laquelle le seuillage est efficace est très limitée. Au delà, le seuillage ne renforce plus le contraste des franges. En deça, il n'y a plus de franges du tout. La dynamique est fortement réduite. En première approximation, on peut imaginer qu'un dégradé original (en haut) ferait apparaître un seuil sur la photo (en bas) :

Coloration orange et voile-miroir
La réaction \[ \ce{AgBr (s) + SCN- (aq) <=> [Ag(SCN)] (aq) + Br- (aq)} \] produit des complexes d'\( \ce{Ag+}\) qui diffusent dans la gélatine. Les révélateurs sont capables de réduire ces \( \ce{Ag+}\) en \( \ce{Ag^0}\), même en dehors des grains, mais avec une efficacité très faible (absence de catalyseur). Il apparait donc quelques atomes d'\( \ce{Ag^0}\) isolés, qui s'agrègent progressivement. Ils peuvent former des agrégats de quelques dizaines d'atomes, en dehors des cristaux, et qui ne vont donc pas grossir beaucoup (il y a peu d'\( \ce{Ag+}\) en dehors des cristaux).
L’argent en solution colloïdale absorbe davantage dans le bleu :
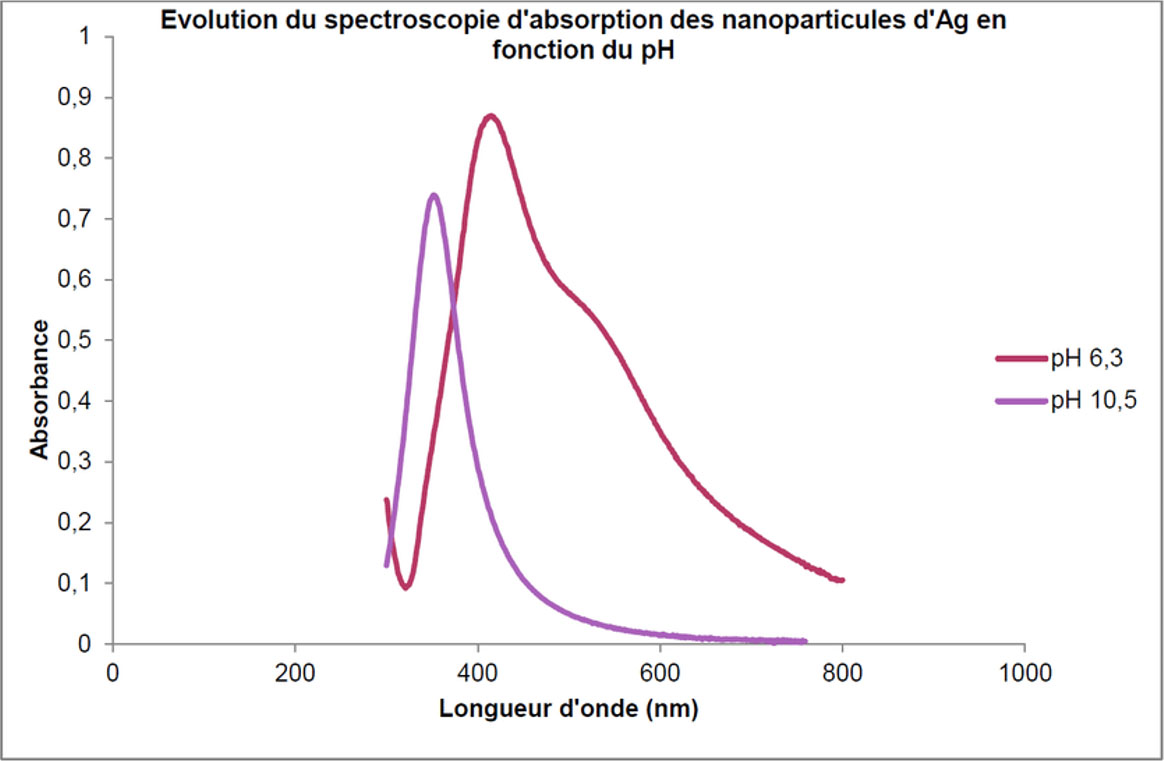
Spectre d'absorbance des suspensions colloïdales de nanoparticules d'argent obtenues par réduction du nitrate d'argent par l'acide ascorbique à deux pH différents (6,3 et 10,5). Source Researchgate.
Les zones avec des petits clusters d’argent colloïdal apparaîtront donc orange par transparence.
Les particules colloïdales ont tendance à s'accumuler aux interfaces (effet Pickering ?). L'interface gélatine/verre est très contrainte, et donc dans le cas présent, c'est l'interface gélatine/air qui aura tendance à piéger les particules colloïdales. L'\( \ce{Ag^0}\) colloïdal diffuse peu, mais l'\( \ce{Ag+}\) diffuse bien (\(D \sim 10^{−6}\,\mathrm{cm^2/s}\), soit 10µm/s). La surface de la gélatine est donc un lieu privilégié de réduction de l'argent, ce qui peut conduire à la création d'une couche fine, voire épaisse (voile uniforme avec effet miroir).
Pour faire disparaître la couleur orange ou le voile miroir, il faut:
- raccourcir le temps de développement ou baisser la température
- baisser la concentration de thiocyanate
- augmenter l’agitation
Composition du GP2
Sources: PF (Photographer formulary); B93 (Silver-Halide Recording Materials for Holography, Bjelkhagen 1993);B14 (The True Colour of Photography de Bjelkhagen et Green);YG20-2 (Yves Gentet, dilution GP2 sans SCN 20/80 + 2ml de SCN dans solution de travail)
Légende: les concentrations sont pour la solution de stock
| PF | B93 | B14 | YG20-2 | |
|---|---|---|---|---|
| Phénidone | 0.2 g/l | 0.2 g/l | 0.2 g/l | ? |
| Hydroquinone | 5 g/l | 5 g/l | 5 g/l | ? |
| Sulfite de sodium | 100 g/l | 100 g/l | 100 g/l | ? |
| Hydroxyde de potassium | 5 g/l | 5 g/l | 5 g/l | ? |
| Thiocyanate d'ammonium | 12 g/l | 12 g/l | 12 g/l | 12 g/l |
| Dilution stock/working | 3.75% | 2.9% | 13% | 20% |
Les recommandations pour la solution de travail avec les produits fournis par Yves Gentet sont variables. La calculateur ci-dessous permet de retrouver la valeur des paramètres standards, en choisissant la valeur de dilution du GP2 sans SCN de stock dans la solution de travail (% GP2-), et la quantité de SCN dosé à 120g/l rajouté dans cette dernière (SCN):
